|

Propietats |
| Nombre atòmic: |
|
85 |
| Massa atòmica
relativa: |
|
[210] uma |
| Punt de fusió: |
|
575 K / 301,84 ºC |
| Punt debullició: |
|
610 K / 336,84 ºC |
| Densitat: |
|
— |
| Estats doxidació: |
|
–1, +1, +3, +5, +7 |
| Electronegativitat
(estat de Pauling): |
|
2,2 |
| Potencial dionització: |
|
9,5 eV |
| Configuració electrònica: |
|
[Xe]4f145d106s26p5 |
| Duresa
(escala de Mohs): |
|
— |
| Potencial normal de reducció: |
|
+0,70 V HAtO | At2 solució àcida |
| Conductivitat tèrmica: |
|
— |
| Conductivitat elèctrica: |
|
— |
| Calor específica: |
|
— |
| Calor de fusió: |
|
2,93 kJ mol–1 |
| Calor devaporació: |
|
— |
| Calor
datomització: |
|
92,0 kJ mol–1 |
| 1a
energia dionització: |
|
890 kJ mol–1 |
| 2a
energia dionització: |
|
— |
| 3a
energia dionització: |
|
— |
| Afinitat electrònica: |
|
270,2 kJ mol–1 |
| Radi atòmic: |
|
1,43 Å |
| Radi covalent: |
|
1,45 Å |
| Radi iònic: |
|
— |
|
— |
|
— |
| Volum atòmic: |
|
— |
| Polaritzabilitat: |
|
6 ų |



|

Fotografia de làstat

Emilio Segrè
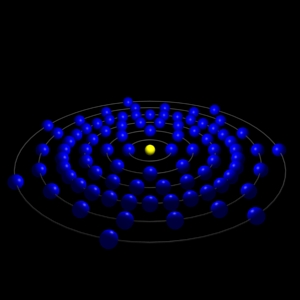
Àtom dàstat ( [Xe]4f145d106s26p5 ) |